ケトン体の新たな受容体は腸管にあった!
国立大学法人東京農工大学大学院農学研究院応用生命化学部門の教授 木村郁夫研究グループの発表で、低炭水化物食や断続的断食がもたらす体脂肪減少効果に、ケトン体の一種であるアセト酢酸とその受容体、そして腸内環境の変化が密接に関わっていることを明らかにしました。
ケトン体とその受容体を介した分子栄養メカニズムの解明は、栄養管理による予防医学とケトン体受容体を標的とした代謝性疾患の改善に期待できます。米国科学アカデミー紀要(PNAS)(2019年11月4日付)に掲載 Ketone body receptor GPR43 regulates lipid metabolism under ketogenic conditions
ケトン体は身体のグルコースが枯渇した状態の時、肝臓で産生され、脳や組織でグルコースの代わりに働くとても、重要なエネルギーなのはご存知ですよね。特に、β-ヒドロキシ酪酸はエネルギー源だけではなく、Gタンパク質共役型受容体であるGPR109AやGPR41を介して情報を伝達する分子として生体生理機能にまで関わることが分かっています。
ですが、もう一つのケトン体(アセト酢酸)の特異的な受容体については発見されておらず、また低炭水化物食や中鎖脂肪酸食のようなケトン体産生が誘導される、ケトン食や断続的断食などは長生きに効率的、また減量効果や脳機能改善など、マウス実験では理解されていました。実際にケトン体によるその詳細な作用機序は不明な部分が多く残されていました。
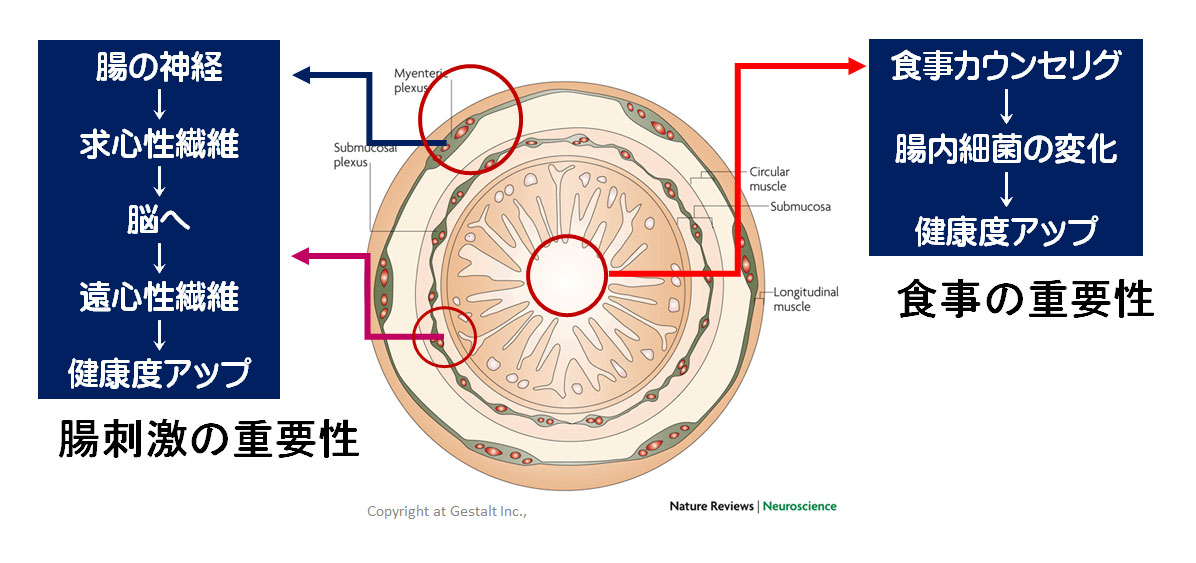
Gタンパク質共役型受容体のひとつGPR43が、ケトン体の一種であるアセト酢酸の受容体であることを新たに発見されたのです。GPR43は短鎖脂肪酸により活性化される受容体だということ。基本的に短鎖脂肪酸は、食事中に含まれる食物繊維等の難消化性多糖類から腸内細菌が醗酵分泌し、私達の身体の代謝や免疫機能に重要な役割を果たしています。
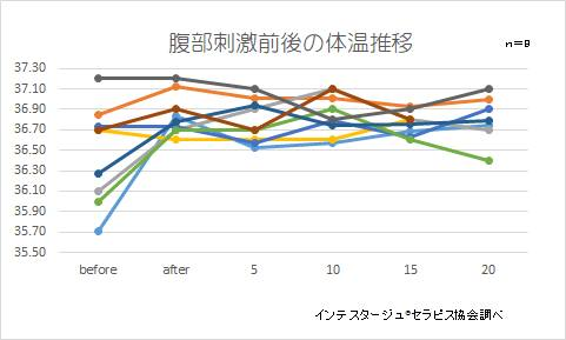
ケトジェニック環境において、血中ケトン体は通常状態の短鎖脂肪酸濃度の10倍以上にも増加します。ようするに、ケトジェニック環境下ではアセト酢酸によりGPR43は活性化されます。一方で、腸管では短鎖脂肪酸の減少によりGPR43が抑制されている状態です。GPR43が抑制されている状態であるということは蠕動運動との兼ね合いがあり、腸セラピーはおすすめだと考えます。
ケトン体であるアセト酢酸によるGPR43刺激が、血中のリポ蛋白質リパーゼの活性を高めることで、中性脂肪の分解を促進し効率的に脂肪酸を組織に取り込む結果、脂質の利用を高めダイエット効果が産まれることになります。GPR43は脂肪細胞上でのインスリンの働きを抑制しますので、糖尿病にたいしてのケトジェニック療法は利用価値がある食事療法だと考えられます。